Ein Kind, das auf den Wasserkocher reagiert: Der kleine Moment, der eine Schlagzeile neu definierte
Sie antwortete ihrer Mutter vom Spülbecken aus: kein klinischer Meilenstein, sondern die Art von gewöhnlicher Szene, die Eltern wie einen Schatz hüten. Vier Monate nach einer einzigen Operation konnte die Siebenjährige einem Gespräch im Haus folgen – sie konnte den Wasserkocher hören. Dieses Bild wurde von Pressematerialien und Schlagzeilen wiederholt aufgegriffen und befeuerte die Formulierung „Gehörlosigkeit rückgängig gemacht“: Wissenschaftler stellen das Gehör bei 10 Patienten nach einer einzigen Injektion wieder her. Es ist eine genaue Beschreibung dessen, was die Studie berichtete, und es ist auch der Punkt, an dem die einfache Geschichte nicht mehr ausreicht.
„Gehörlosigkeit rückgängig gemacht“: Wissenschaftler stellen Gehör wieder her – die Zahlen hinter den Schlagzeilen
An der Studie nahmen zehn Teilnehmer im Alter von 1 bis 24 Jahren teil. Über die gesamte Kohorte hinweg sank der durchschnittliche Schallpegel, den die Patienten wahrnehmen konnten, innerhalb von sechs Monaten von etwa 106 Dezibel auf 52 Dezibel – eine Veränderung, die einen extremen Hörverlust in einen Bereich verwandelt, in dem für viele Menschen eine normale Konversation möglich ist. Die Verbesserungen traten oft rasch ein: Bei mehreren Patienten zeigten sich bereits nach einem Monat erste Funktionen, und die jüngsten Kinder – insbesondere die im Alter von fünf bis acht Jahren – erzielten die größten Fortschritte. Eine Siebenjährige erlangte ein nahezu vollständig funktionierendes Gehör zurück und war in der Lage, am Telefon zu sprechen und tägliche Gespräche mit der Familie zu führen.
Diese Zahlen erklären, warum die Presse die Worte „Gehörlosigkeit rückgängig gemacht“ verwendete und warum Eltern und Mediziner begeistert sind. Sie enthalten jedoch auch einen offensichtlichen statistischen Vorbehalt: Zehn Personen sind immer noch eine kleine Stichprobe. Bei der Studie handelt es sich um eine einarmige Studie ohne randomisierte Kontrolle, und die Nachbeobachtung ist bisher auf Monate statt auf Jahre begrenzt. Das Ergebnis ist ein eindrucksvoller Beleg für die biologische Plausibilität bei dieser spezifischen Mutation, aber noch keine universelle Heilung.
„Gehörlosigkeit rückgängig gemacht“: Wissenschaftler stellen Gehör wieder her – beschränkt auf OTOF, und das ist entscheidend
Die behandelten Patienten teilten alle die gleiche molekulare Diagnose: biallele Funktionsverlustmutationen in OTOF, dem Gen, das für Otoferlin kodiert – ein Protein, das entscheidend für die synaptische Übertragung von Schallinformationen von den inneren Haarzellen an den Hörnerv ist. Die Einschleusung einer korrekten Kopie von OTOF in diese Haarzellen stellte diese Kommunikation wieder her und führte zu den berichteten messbaren Verbesserungen.
Der operative Moment und die in der Fachpublikation beschriebene Biologie
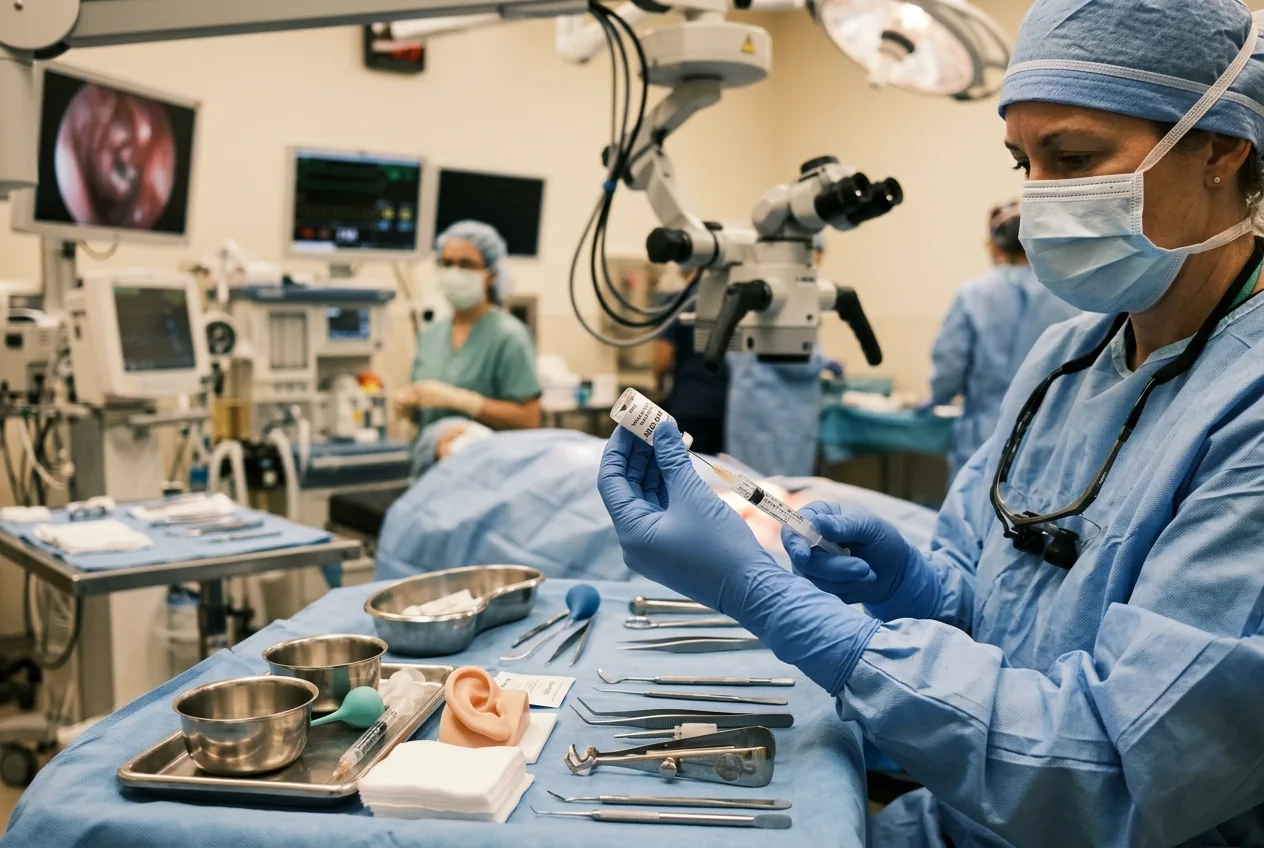
Das Verfahren in der Studie war chirurgisch und lokal begrenzt: Mediziner injizierten einen AAV-basierten Vektor, der eine funktionelle OTOF-Sequenz trägt, durch die Membran des runden Fensters in die Cochlea. Das Innenohr ist ein begrenzter, empfindlicher Raum; die Operation erfordert otologisch-chirurgisches Geschick und bildgebende Verfahren. Die Studienteams berichten, dass die Intervention allgemein gut vertragen wurde. Die häufigste laborchemische Veränderung war eine vorübergehende Verringerung der Neutrophilenzahlen, und entscheidend ist, dass während des sechs- bis zwölfmonatigen Nachbeobachtungszeitraums keine schwerwiegenden unerwünschten Ereignisse gemeldet wurden.
Dieses Sicherheitsprofil muss genau beobachtet werden. Adeno-assoziierte virale Vektoren werden in der Gentherapie häufig eingesetzt, da sie vergleichsweise harmlos sind, aber das geringe Volumen der Cochlea und die Nähe der behandelten Zellen zum Zentralnervensystem werfen spezifische Fragen zu Dosis, Immunantwort und Langzeitexpression auf. Weder die Studie noch die Publikation können bisher beantworten, wie dauerhaft die Wirkung über Jahre oder Jahrzehnte sein wird, ob wiederholte Dosierungen erforderlich sein werden oder wie eine bilaterale (beidseitige) Behandlung im Vergleich zur unilateralen Dosierung abschneidet.
Kommerzielle Verflechtungen, Konflikte und der Wettlauf um die Behandlung verbreiteter Schwerhörigkeit
Über Interessenkonflikte hinaus gibt es eine eher systemische Spannung. Jede genetische Form der Gehörlosigkeit wird eine eigene, maßgeschneiderte Behandlung benötigen: neue Vektoren, neue Herstellungsverfahren, spezifische chirurgische Protokolle und neue Sicherheitsdossiers. Diese maßgeschneiderte Natur ist der Grund, warum viele Gruppen – darunter Rinri Therapeutics an der University of Sheffield – einen anderen Weg einschlagen und aus Stammzellen gewonnene Vorläuferzellen des Hörnervs entwickeln, die auf eine breitere Klasse sensorineuraler Verluste abzielen. Zelltherapien versprechen eine breitere Anwendbarkeit, bringen aber ihre eigenen Hürden bei Regulierung, Herstellung und Verabreichung mit sich. Die wirtschaftlichen Aspekte sind drastisch: Personalisierte Genmedikamente und komplexe Zellprodukte sind teuer in der Entwicklung und Skalierung. Wer die Kosten übernimmt und wie schnell die Aufsichtsbehörden die neuen Ansätze akzeptieren werden, bleibt offen.
Ist die Behandlung jetzt verfügbar – und was sind die tatsächlichen Risiken?
Kurze Antwort: Nein, nicht für den routinemäßigen klinischen Einsatz. Die Studie in Nature Medicine ist ein früher klinischer Schritt. Das Produkt bleibt experimentell, und der Weg zu einer breiteren Zulassung führt über größere multizentrische Studien, die einen dauerhaften Nutzen, akzeptable Sicherheit in verschiedenen Bevölkerungsgruppen, eine reproduzierbare Herstellung sowie Klarheit über Kosten und Zugang belegen. Für Familien, welche die Schlagzeilen hören, kann das eine unangenehme Nachricht sein: Die Wissenschaft ist real, und die Therapie hat bei diesen Patienten funktioniert, aber die Verfügbarkeit für die Öffentlichkeit wird weitere Studien und behördliche Prüfungen erfordern.
Was die Risiken betrifft, so zeigte die veröffentlichte Nachbeobachtung im ersten Jahr keine schwerwiegenden Nebenwirkungen. Kliniker und Aufsichtsbehörden werden jedoch auf späte Immunreaktionen, Off-Target-Expressionen und die Unwägbarkeiten der langfristigen Cochlea-Biologie nach einer genetischen Wiederherstellung achten. Hinzu kommt das praktische chirurgische Risiko beim Zugang zur Cochlea sowie die Möglichkeit, dass Patienten, welche die Behandlung in höherem Alter erhalten, aufgrund einer langjährigen neuronalen Deprivation weniger profitieren als Kinder.
Einordnung in den langfristigen Weg zur Wiederherstellung des Gehörs für Millionen
Die Studie ist ein Wendepunkt: Sie beweist, dass eine Gentherapie sicher in die menschliche Cochlea verabreicht werden kann und bei einer genetischen Untergruppe zu schnellen, bedeutsamen Fortschritten führt. Das ist selten und wichtig. Doch die Medizingeschichte ist voll von frühen Wundern, die sich nur schwer verallgemeinern ließen. Die nächsten Schritte werden pragmatisch, teuer und langsam sein: die Skalierung der Produktion, die Durchführung randomisierter Studien, die Sicherung der behördlichen Zulassung in mehreren Ländern und der Aufbau chirurgischer und audiologischer Systeme zur Verabreichung und Überwachung einer neuen Klasse von Behandlungen.
In der Zwischenzeit zielen komplementäre Wege wie das Neuronenersatzprogramm Rincell-1 von Rinri auf den größeren Markt der sensorineuralen Hörverluste durch Alterung und Lärmschäden ab. Diese Technologien könnten, wenn sie erfolgreich sind, mehr Menschen erreichen, stehen aber vor eigenen Hürden beim Wirksamkeitsnachweis und der Verabreichung. Die unmittelbare Lehre daraus ist, dass das Feld nun legitimerweise zweigeteilt ist: gezielte Genkorrekturen für spezifische monogene Taubheit und breitere regenerative Ansätze für erworbene oder komplexe Formen.
Der Wasserkocher in einer Küche ist immer noch ein guter Maßstab für Bedeutung. Für die Familien der Studienteilnehmer führte eine einzige Operation innerhalb von Monaten zu lebensverändernden Verbesserungen. Für den Rest der Welt ist die Schlagzeile „Gehörlosigkeit rückgängig gemacht“: Wissenschaftler stellen Gehör wieder her eher ein Versprechen im Entstehen als eine abgeschlossene Geschichte. Die sorgfältige Arbeit konzentriert sich nun auf Dauerhaftigkeit, Skalierbarkeit, Gerechtigkeit und unabhängige Replikation; die sehr praktische Frage ist, ob Aufsichtsbehörden und Gesundheitssysteme einen eleganten, genspezifischen Erfolg in einen fairen, dauerhaften Zugang für diejenigen verwandeln können, die ihn benötigen.
Quellen
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (Pressematerialien und institutionelle Forschungskommunikation)
- Zhongda Hospital, Southeast University (klinische Kooperationspartner)
- Rinri Therapeutics / University of Sheffield (Rincell-1 und regeneratives Zelltherapieprogramm)
- Otovia Therapeutics (an der Studie beteiligter Entwickler und Geldgeber)
Kommentare
Noch keine Kommentare. Seien Sie der Erste!