Ett barn som reagerar på vattenkokaren: det lilla ögonblicket som omformade en rubrik
Hon svarade sin mamma från diskbänken: inte en klinisk milstolpe, utan den sortens vardagliga scen som föräldrar bär med sig. Fyra månader efter en enda operation kunde sjuåringen följa ett samtal i hemmet – hon kunde höra vattenkokaren. Den bilden har återkommande återanvänts i pressmaterial och rubriker, och den bidrog till frasen ”dövhet hävd”: forskare återställer hörseln hos 10 patienter efter en injektion. Det är en korrekt beskrivning av vad studien rapporterade, och det är också där den enkla berättelsen slutar vara tillräcklig.
”dövhet hävd”: forskare återställer – siffrorna som skapar rubriker
Studien omfattade tio deltagare i åldrarna 1 till 24 år. Inom kohorten sjönk den genomsnittliga ljudnivån som patienterna kunde uppfatta från cirka 106 decibel till 52 decibel inom sex månader – en förändring som omvandlar extrem hörselnedsättning till ett intervall där konversationstal är möjligt för många människor. Förbättringarna var ofta snabba: flera patienter började uppvisa funktion efter bara en månad, och de yngsta barnen – särskilt de i åldrarna fem till åtta – uppvisade de största vinsterna. En sjuåring återfick nästan full funktionell hörsel och kunde prata i telefon och föra dagliga samtal med familjen.
Dessa siffror förklarar varför pressen använde orden ”dövhet hävd” och varför föräldrar och kliniker är hoppfulla. De innehåller också ett uppenbart statistiskt förbehåll: tio personer är fortfarande ett litet urval. Studien är en enarmad studie utan randomiserad kontroll, och uppföljningen är hittills begränsad till månader snarare än år. Resultatet är en kraftfull demonstration av biologisk rimlighet för denna specifika mutation, men ännu inte ett universellt botemedel.
”dövhet hävd”: forskare återställer – begränsat till OTOF, och det spelar roll
De behandlade patienterna delade alla samma molekylära diagnos: bialleliska funktionsförlustmutationer i OTOF, genen som kodar för otoferlin, ett protein som är avgörande för den synaptiska överföringen av ljudinformation från inre hårceller till hörselnerven. Att leverera en korrekt kopia av OTOF till dessa hårceller återställde den kommunikationen och gav de mätbara förbättringar som rapporterats.
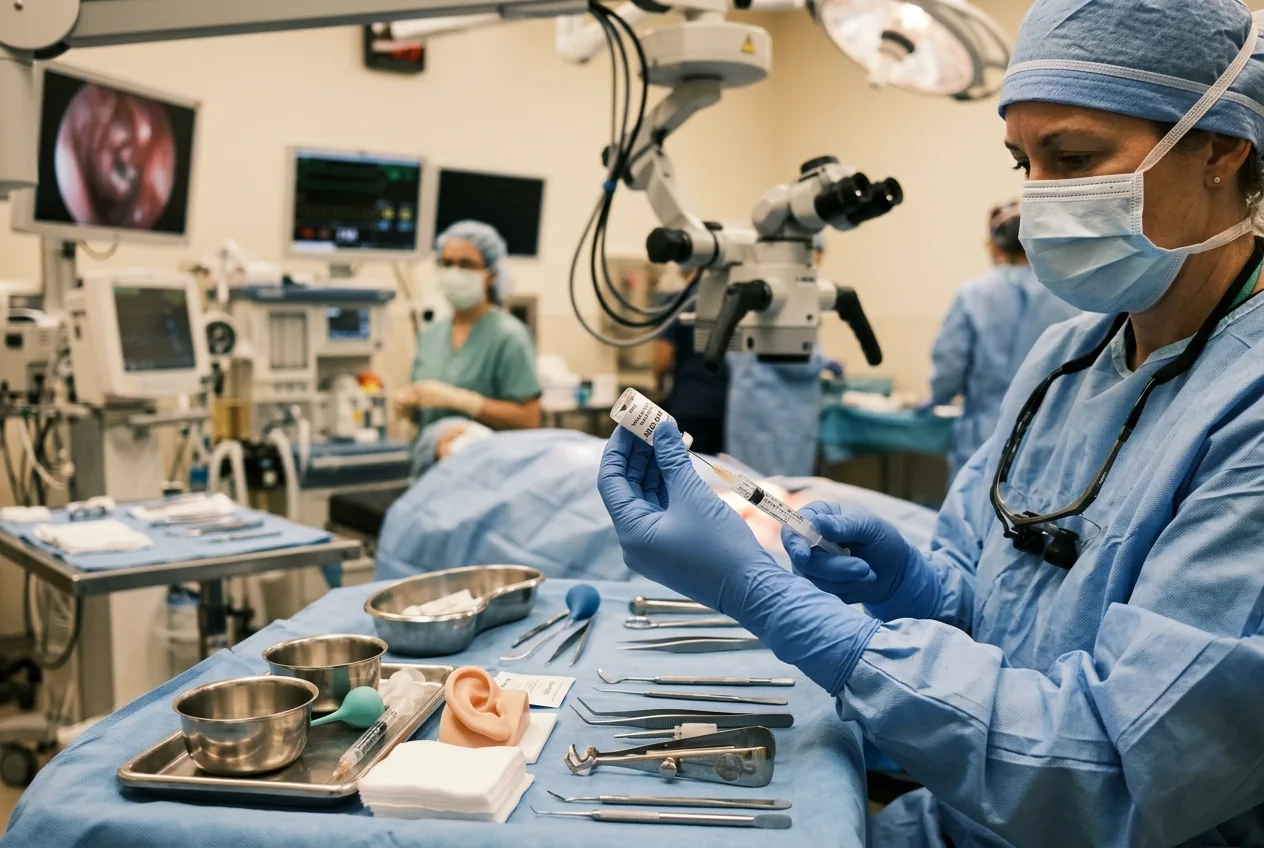
Det operativa ögonblicket och biologin som rapporteras i artikeln
Proceduren i studien var kirurgisk och lokal: kliniker injicerade en AAV-baserad vektor som bar på en funktionell OTOF-sekvens genom runda fönstrets membran in i snäckan (cochlean). Innerörat är ett avgränsat, känsligt utrymme; operationen kräver otokirurgisk skicklighet och bilddiagnostik. Studieteamen rapporterar att interventionen generellt tolererades väl. Den vanligaste laboratorieförändringen var en tillfällig minskning av antalet neutrofiler och, avgörande nog, rapporterades inga allvarliga biverkningar under uppföljningsperioden på sex till tolv månader.
Denna säkerhetsprofil kommer att behöva övervakas noga. Adenoassocierade virusvektorer (AAV) används i stor utsträckning i genterapier eftersom de är jämförelsevis godartade, men snäckans lilla volym och de behandlade cellernas närhet till centrala nervsystemet väcker specifika frågor om dos, immunsvar och långsiktigt uttryck. Varken studien eller artikeln kan ännu svara på hur hållbar effekten kommer att vara över år eller decennier, om upprepad dosering kommer att behövas eller hur bilateral behandling (båda öronen) presterar jämfört med unilateral dosering.
Kommersiella band, konflikter och kapplöpningen för att behandla vanlig dövhet
Utöver intressekonflikter finns en mer systemisk spänning. Varje genetisk form av dövhet kommer att behöva sin egen skräddarsydda behandling: nya vektorer, ny tillverkning, specialanpassade kirurgiska protokoll och nya säkerhetsunderlag. Denna specialanpassade natur är anledningen till att många grupper – inklusive Rinri Therapeutics vid University of Sheffield – följer en annan väg och utvecklar stamcellsderiverade förstadier till hörselnerver som siktar på en bredare klass av sensorineurala hörselnedsättningar. Cellterapier lovar bredare tillämpbarhet, men de för med sig egna regulatoriska, tillverkningsmässiga och leveransrelaterade hinder. Ekonomin är kärv: personliga genläkemedel och komplexa cellprodukter är dyra att utveckla och skala upp. Vem som ska betala, och hur snabbt tillsynsmyndigheter kommer att acceptera de nya metoderna, förblir öppna frågor.
Är behandlingen tillgänglig nu – och vilka är de verkliga riskerna?
Kort svar: nej, inte för rutinmässig klinisk användning. Studien i Nature Medicine är ett tidigt kliniskt steg. Produkten förblir experimentell, och vägen till ett bredare godkännande innefattar större multicenterstudier som visar på hållbar nytta, acceptabel säkerhet i olika populationer, reproducerbar tillverkning samt tydlighet kring kostnad och tillgång. För familjer som hör rubrikerna kan det vara ett obekvämt budskap: vetenskapen är verklig och terapin fungerade för dessa patienter, men tillgänglighet för allmänheten kommer att kräva ytterligare studier och regulatorisk granskning.
När det gäller risker visade den publicerade uppföljningen inga allvarliga biverkningar under det första året, men kliniker och tillsynsmyndigheter kommer att leta efter sena immuneffekter, off-target-uttryck och de okända faktorerna i den långsiktiga biologin i snäckan efter genetisk återställning. Det finns också den praktiska kirurgiska risken med att få tillgång till snäckan och möjligheten att patienter som får behandlingen vid äldre ålder kommer att vinna mindre än barn på grund av långvarig neural deprivation.
Var detta placerar sig i den längre utvecklingen mot att återställa hörseln för miljoner
Studien är en vändpunkt: den bevisar att en genterapi kan levereras säkert in i den mänskliga snäckan och ge snabba, betydelsefulla vinster för en genetisk undergrupp. Det är sällsynt och viktigt. Men medicinhistorien är fylld av tidiga mirakel som visade sig svåra att generalisera. Nästa steg kommer att vara pragmatiska, dyra och långsamma: att skala upp tillverkningen, genomföra randomiserade studier, säkra regulatoriska godkännanden i flera jurisdiktioner och bygga kirurgiska och audiologiska system för att leverera och övervaka en ny klass av behandlingar.
Samtidigt siktar kompletterande vägar, såsom Rinris nervcellsersättningsprogram Rincell-1, på den större marknaden för sensorineural hörselnedsättning till följd av åldrande och bullerskador. Om dessa tekniker lyckas skulle de kunna nå fler människor, men de kommer att möta sina egna hinder gällande ”proof-of-concept” och leverans. Den omedelbara lärdomen är att fältet nu är legitimt uppdelat: riktade genfixar för specifik monogen dövhet och bredare regenerativa metoder för förvärvade eller komplexa former.
Vattenkokaren i ett kök är fortfarande ett bra sätt att mäta betydelse. För familjerna till deltagarna i studien gav en enda operation livsavgörande förändringar inom några månader. För resten av världen är rubriken ”dövhet hävd”: forskare återställer ett löfte under utveckling snarare än en avslutad historia. Det noggranna arbetet nu handlar om hållbarhet, skala, rättvisa och oberoende replikering; den mycket praktiska frågan är om tillsynsmyndigheter och hälsosystem kan omvandla en elegant, genspecifik framgång till rättvis och varaktig tillgång för dem som behöver den.
Källor
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single-arm trial)
- Karolinska Institutet (pressmaterial och institutionell forskningskommunikation)
- Zhongda Hospital, Southeast University (kliniska samarbetspartners)
- Rinri Therapeutics / University of Sheffield (Rincell-1 och regenerativt cellterapiprogram)
- Otovia Therapeutics (utvecklare och finansiär involverad i studien)
Comments
No comments yet. Be the first!