Dziecko reagujące na czajnik: mała chwila, która nadała nowy wymiar nagłówkowi
Odpowiedziała matce, stojąc przy zlewie kuchennym: to nie kamień milowy w badaniach klinicznych, ale rodzaj zwyczajnej sceny, którą rodzice zachowują głęboko w pamięci. Cztery miesiące po jednej operacji siedmiolatka mogła śledzić rozmowę w domu — słyszała czajnik. Ten obraz był wielokrotnie powielany przez materiały prasowe i nagłówki, co pomogło wypromować frazę „odwrócenie głuchoty”: naukowcy przywracają słuch u 10 pacjentów po jednym zastrzyku. Jest to trafny opis tego, co wykazało badanie, i zarazem punkt, w którym prosta opowieść przestaje wystarczać.
„odwrócenie głuchoty”: naukowcy przywracają słuch — liczby, które trafiają na czołówki
W badaniu wzięło udział dziesięciu uczestników w wieku od 1 do 24 lat. W całej grupie średni poziom dźwięku postrzegany przez pacjentów spadł z około 106 decybeli do 52 decybeli w ciągu sześciu miesięcy — to zmiana, która przekształca głęboką utratę słuchu w zakres, w którym dla wielu osób możliwa jest mowa potoczna. Poprawa była często szybka: u kilku pacjentów funkcje słuchowe zaczęły powracać już po miesiącu, a największe korzyści odniosły najmłodsze dzieci — zwłaszcza te w wieku od pięciu do ośmiu lat. Pewna siedmiolatka odzyskała niemal pełny słuch funkcjonalny i była w stanie rozmawiać przez telefon oraz prowadzić codzienne rozmowy z rodziną.
Dane te wyjaśniają, dlaczego prasa użyła sformułowania „odwrócenie głuchoty” i dlaczego rodzice oraz klinicyści są podekscytowani. Zawierają one jednak również oczywiste zastrzeżenie statystyczne: dziesięć osób to wciąż mała próba. Badanie jest próbą jednoramienną, bez randomizowanej grupy kontrolnej, a okres obserwacji ograniczony jest na razie do miesięcy, a nie lat. Wynik jest potężną demonstracją biologicznej wiarygodności terapii dla tej konkretnej mutacji, ale nie jest jeszcze uniwersalnym lekarstwem.
„odwrócenie głuchoty”: naukowcy przywracają słuch — ograniczenie do OTOF i dlaczego ma to znaczenie
Wszyscy leczeni pacjenci mieli tę samą diagnozę molekularną: bialleliczne mutacje powodujące utratę funkcji w genie OTOF, kodującym otoferlinę — białko kluczowe dla synaptycznego przesyłania informacji dźwiękowych z wewnętrznych komórek rzęsatych do nerwu słuchowego. Dostarczenie prawidłowej kopii genu OTOF do tych komórek rzęsatych przywróciło tę komunikację i przyniosło opisaną mierzalną poprawę.
Moment operacji i biologia opisana w publikacji
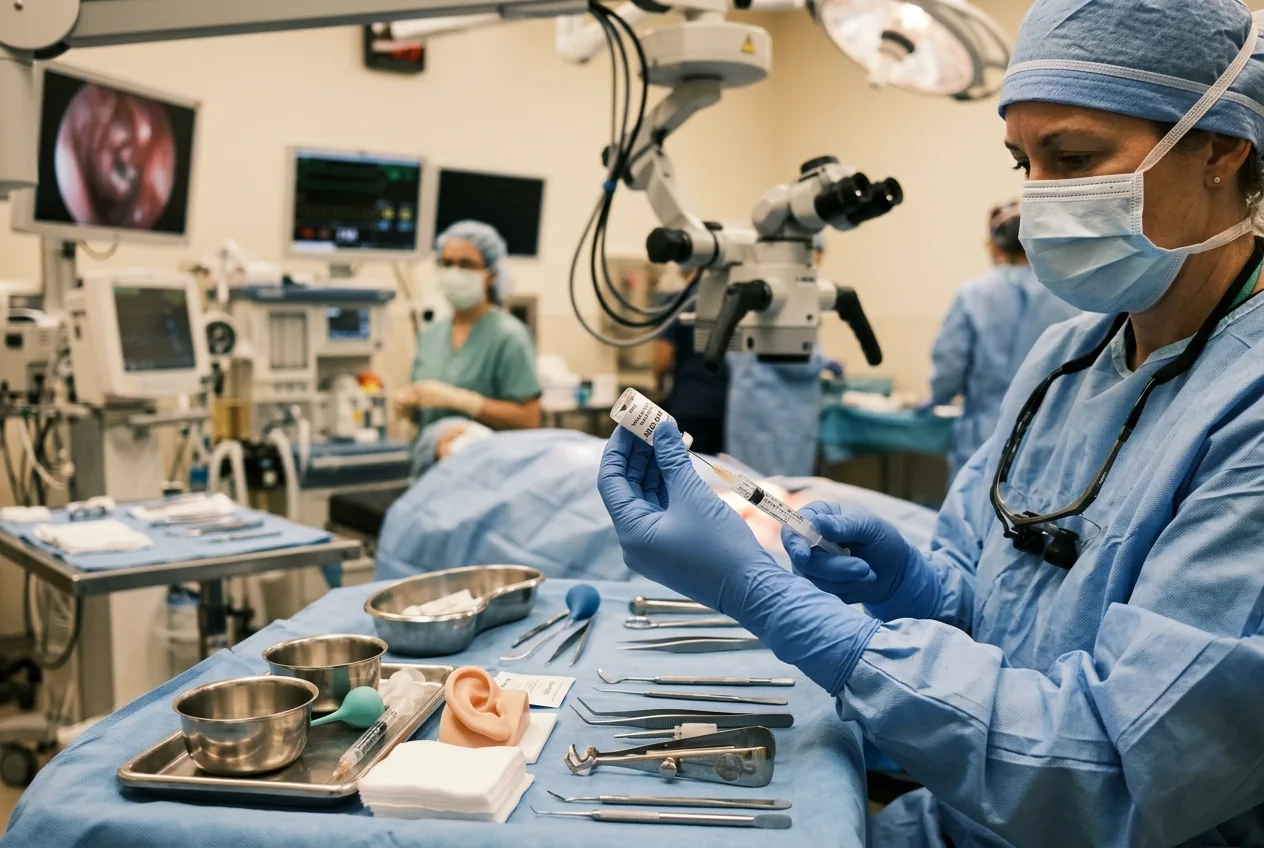
Procedura w badaniu miała charakter chirurgiczny i miejscowy: klinicyści wstrzyknęli wektor oparty na AAV, niosący funkcjonalną sekwencję OTOF, przez błonę okienka okrągłego do ślimaka. Ucho wewnętrzne to ograniczona, delikatna przestrzeń; operacja wymaga umiejętności z zakresu chirurgii otologicznej i diagnostyki obrazowej. Zespoły badawcze informują, że interwencja była ogólnie dobrze tolerowana. Najczęstszą zmianą laboratoryjną była przejściowa redukcja liczby neutrofili i, co kluczowe, nie zgłoszono żadnych poważnych zdarzeń niepożądanych w ciągu sześcio- do dwunastomiesięcznego okresu obserwacji.
Ten profil bezpieczeństwa będzie musiał być ściśle monitorowany. Wektory wirusowe oparte na wirusach towarzyszących adenowirusom (AAV) są szeroko stosowane w terapiach genowych, ponieważ są stosunkowo łagodne, ale niewielka objętość ślimaka i bliskość leczonych komórek względem ośrodkowego układu nerwowego budzą konkretne pytania o dawkę, odpowiedź immunologiczną i długoterminową ekspresję. Ani badanie, ani publikacja nie dają jeszcze odpowiedzi na pytanie, jak trwały będzie ten efekt w skali lat lub dekad, czy potrzebne będzie powtórne dawkowanie, ani jak leczenie obustronne (w obu uszach) wypada w porównaniu z dawkowaniem jednostronnym.
Powiązania komercyjne, konflikty interesów i wyścig o leczenie powszechnej głuchoty
Poza konfliktami interesów istnieje głębsze napięcie systemowe. Każda genetyczna forma głuchoty będzie wymagała własnego, dostosowanego leczenia: nowych wektorów, nowej produkcji, spersonalizowanych protokołów chirurgicznych i nowych dokumentacji bezpieczeństwa. Ta specyfika sprawia, że wiele grup — w tym Rinri Therapeutics na University of Sheffield — przyjmuje inną strategię, opracowując pochodzące z komórek macierzystych komórki progenitorowe nerwu słuchowego, skierowane na szerszą klasę niedosłuchów czuciowo-nerwowych. Terapie komórkowe obiecują szersze zastosowanie, ale niosą ze sobą własne przeszkody regulacyjne, produkcyjne i logistyczne. Ekonomia jest nieubłagana: spersonalizowane leki genowe i złożone produkty komórkowe są kosztowne w opracowaniu i skalowaniu. Kwestie tego, kto za to zapłaci i jak szybko organy regulacyjne zaakceptują nowe podejścia, pozostają pytaniami otwartymi.
Czy leczenie jest już dostępne — i jakie są rzeczywiste zagrożenia?
Krótka odpowiedź brzmi: nie, nie do rutynowego użytku klinicznego. Badanie opublikowane w Nature Medicine to wczesny krok kliniczny. Produkt pozostaje eksperymentalny, a droga do szerszego zatwierdzenia wiedzie przez większe badania wieloośrodkowe, które wykażą trwałe korzyści, akceptowalne bezpieczeństwo w zróżnicowanych populacjach, powtarzalność produkcji oraz jasność w kwestii kosztów i dostępu. Dla rodzin śledzących nagłówki może to być trudny komunikat: nauka jest prawdziwa, a terapia zadziałała u tych pacjentów, ale dostępność dla opinii publicznej będzie wymagała dodatkowych badań i przeglądu regulacyjnego.
Jeśli chodzi o ryzyko, opublikowana obserwacja nie wykazała poważnych reakcji niepożądanych w pierwszym roku, ale klinicyści i organy regulacyjne będą wypatrywać późnych efektów immunologicznych, ekspresji poza docelowym miejscem oraz niewiadomych dotyczących długoterminowej biologii ślimaka po przywróceniu funkcji genetycznych. Istnieje również praktyczne ryzyko chirurgiczne związane z dostępem do ślimaka oraz możliwość, że pacjenci otrzymujący leczenie w starszym wieku zyskają mniej niż dzieci z powodu długotrwałej deprywacji neuronowej.
Miejsce tego odkrycia w długiej drodze do przywrócenia słuchu milionom ludzi
To badanie jest punktem zwrotnym: udowadnia, że terapia genowa może być bezpiecznie dostarczona do ludzkiego ślimaka i przynieść szybką, znaczącą poprawę w podgrupie genetycznej. Jest to rzadkie i ważne osiągnięcie. Jednak historia medycyny jest pełna wczesnych cudów, które okazały się trudne do upowszechnienia. Następne kroki będą pragmatyczne, kosztowne i powolne: skalowanie produkcji, prowadzenie badań randomizowanych, uzyskiwanie zatwierdzeń regulacyjnych w wielu jurysdykcjach oraz budowanie systemów chirurgicznych i audiologicznych do dostarczania i monitorowania nowej klasy zabiegów.
W międzyczasie komplementarne ścieżki, takie jak program wymiany neuronów Rincell-1 firmy Rinri, celują w większy rynek niedosłuchu czuciowo-nerwowego wynikającego ze starzenia się i uszkodzeń spowodowanych hałasem. Technologie te, jeśli odniosą sukces, mogą dotrzeć do większej liczby osób, ale zmierzą się z własnymi przeszkodami w zakresie potwierdzenia koncepcji i dostarczania leku. Doraźna lekcja jest taka, że dziedzina ta uległa obecnie wyraźnemu rozwidleniu: na ukierunkowane poprawki genowe dla specyficznej głuchoty monogenowej oraz szersze podejścia regeneracyjne dla form nabytych lub złożonych.
Czajnik w kuchni to wciąż dobry sposób na mierzenie znaczenia sukcesu. Dla rodzin uczestników badania jedna operacja przyniosła zmiany zmieniające życie w ciągu kilku miesięcy. Dla reszty świata nagłówek „odwrócenie głuchoty”: naukowcy przywracają słuch jest obietnicą w trakcie realizacji, a nie skończoną historią. Obecna, staranna praca skupia się na trwałości, skali, równości i niezależnej replikacji; bardzo praktycznym pytaniem jest to, czy organy regulacyjne i systemy opieki zdrowotnej zdołają przekształcić elegancki, specyficzny dla danego genu sukces w sprawiedliwy i trwały dostęp dla tych, którzy go potrzebują.
Źródła
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (materiały prasowe i komunikaty naukowe instytucji)
- Zhongda Hospital, Southeast University (współpracownicy kliniczni)
- Rinri Therapeutics / University of Sheffield (Rincell-1 i program regeneracyjnej terapii komórkowej)
- Otovia Therapeutics (deweloper i fundator zaangażowany w badanie)
Comments
No comments yet. Be the first!