リード:注射器、DNA、そして消える武器
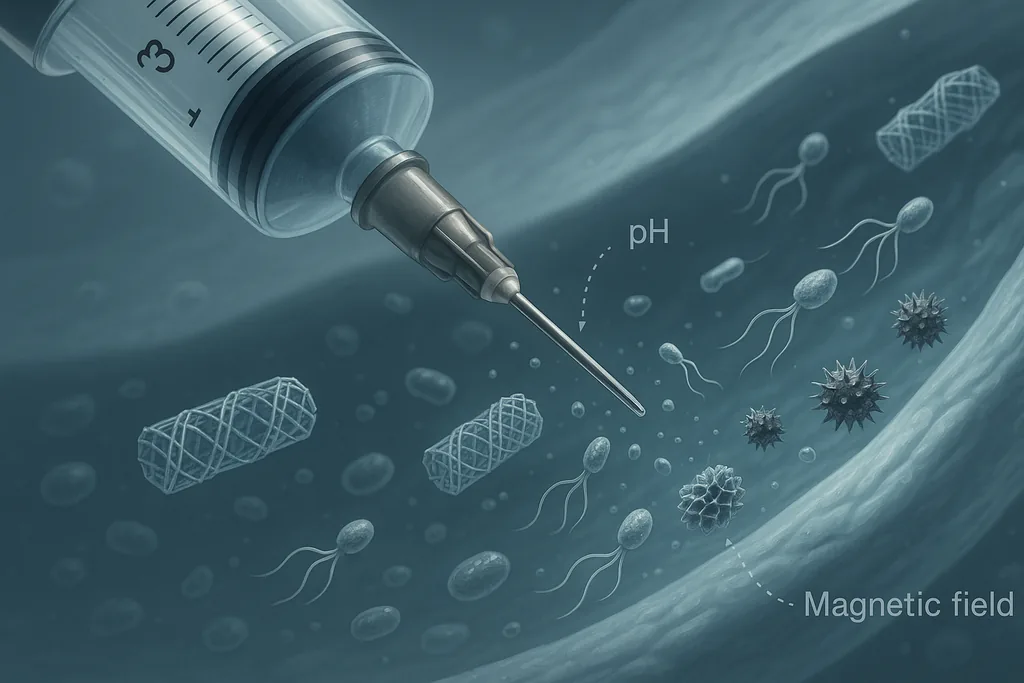
Karolinska Institutetの研究室で、研究者たちはDNAの鎖を折り畳んでウイルスほどの幅の空洞のチューブを作り、その内部にペプチドの「武器」を格納し、この組み立て体を乳腺腫瘍を持つマウスに注入した。このペプチドは、ナノ構造体が血液中を循環している間は隠されていたが、腫瘍を取り巻く酸性の微小環境において展開し、その致死的なパターンを露呈させた。その結果、不活性な対照群と比較して、動物の腫瘍増殖を約70%抑制することに成功した。Nature Nanotechnology誌に掲載され、今年大学のプレスリリースで発表されたこの研究は、「ナノロボット」としばしば称される構造体が、生体内で標的を絞った動作を実行できることを示す、いくつかの目覚ましい実証例の一つである。
異なるタイプの注入型ナノマシン
他のチームは、泳ぐバイオハイブリッド・マイクロロボットを追求している。カリフォルニア大学サンディエゴ校の研究者たちは、薬剤を充填したナノ粒子を運動性のある藻類に付着させ、肺組織の奥深くや転移結節へと荷物を運ぶことができる小さなスイマーを作り出した。マウスを用いた実験では、これらのスイマーは対照群と比較して腫瘍の拡散を遅らせ、生存率を向上させた。これらのシステムは(ナノメートルスケールではなくマイクロメートルスケールと)より大きく、純粋な分子の折り畳みではなく、天然の推進力を利用している。
「ロボット」という名称が役立つ場面、そして誤解を招く場面
これらのデバイスを「ロボット」と呼ぶことは、修辞的には強力だが、技術的な実態を曖昧にする可能性がある。マクロスケールのロボットとは異なり、ほとんどの注入型デザインは、プロセッサ、モーター、バッテリーを搭載していない。それらの知性は通常、化学からきている。すなわち、分子的な合図に反応して立体構造を変化させるDNAやタンパク質の配列、あるいは磁石による物理的な操作である。これらの挙動はプログラム可能で再現性があるが、自律的な認知ではない。ミニチュアのアンドロイドというよりは、条件付きのドラッグデポ(薬剤貯蔵庫)に近い。それでも、この用語は、これらの構築物が感知し、形状を変化させ、その場で治療効果を発動できるという、少し前まではSFの世界の話であった一連の能力を的確に捉えている。
動物実験の結果が有望でありながら決定的ではない理由
マウスによる研究は不可欠な第一歩だが、いくつかの極めて重要な疑問が未解決のまま残されている。マウスの腫瘍モデルは、人間の癌よりも脈管構造や免疫環境が単純であることが多く、大型動物や人間に移行する際、生体内分布、オフターゲットへの蓄積、全身の免疫反応が劇的に異なる可能性がある。DNAベースのデバイスにとって、血液中のヌクレアーゼによる分解、意図しない免疫認識、そして安全で一貫した大規模製造は実用上の障害である。バイオハイブリッドや磁気システムについては、長期的な生体適合性、塞栓のリスク、そして臨床的に意味のある割合の腫瘍組織に十分な活性ペイロードを届ける能力が未解決の課題となっている。研究者たちもこれらの格差を認めており、pH活性化DNAナノ構造体やトロンビン・ナノロボットを開発したチームは、いずれもヒトでの治験の前に、より高度な疾患モデルでの試験と徹底的な安全性調査を求めている。
製造、安定性、および規制の障壁
ナノスケールシステムを医薬品として実用化するには、再現性が高く高収率な生産と、厳格な品質管理が必要である。DNAオリガミは現在、長い足場鎖と多くの短いステープル・オリゴヌクレオチドに依存している。足場鎖の経路を節約しステープル配列を再利用する技術が進歩しても、コストとプロセス管理は依然として軽視できない課題である。最近の工学的取り組みにより、複雑さが軽減され組み立てルールが改善されたが、臨床利用のための製造には、純度、エンドトキシン管理、バッチ間の一貫性に関する新たな基準が必要となる。また、規制当局は明確な作用機序と安全マージンを要求するだろう。例えば、意図的に局所的な凝固を誘発するデバイスは、全身性の凝固を確実に回避することを証明しなければならない。この分野は、これらの実証を日常的なものにするための技術的および規制的なツールキットを、今まさに構築している段階にある。
臨床への道筋と予想されるタイムライン
すべての手法が、臨床利用に向けて同じ道のりを辿るわけではない。既知の生物学的製剤を再利用したシンプルなペイロード送達システムは、完全に新規の分子マシンよりも早く規制の門を通過する可能性がある。外部制御(磁気、超音波)を使用するデバイスは、確立された画像診断や介入プラットフォームに便乗できるため、安全性が示されれば臨床開発期間を短縮できる可能性がある。多くの研究者は、段階的な実用化を予測している。まず、局所的またはex vivoでの利用(手術中の標的血栓形成など)、次に選択肢の限られた患者を対象とした厳格に管理された画像誘導下での治験、そして安全性と有効性が確認されれば、より広範な適応症へと進むという流れである。
この分野に携わる研究者による現実的な予測では、ほとんどのコンセプトにおいてヒトでの初回治験までに数ヶ月ではなく数年を要するとされている。楽観的な道筋であっても、数年にわたる毒性試験、スケールアップされた製造、および規制当局との連携が必要である。しかし、ここ数年で複数の機関にわたっていくつもの異なる生体内実証が行われたという進歩のペースは、臨床的に有用な注入型ナノマシンというアイデアが、単なる空想ではなく、中長期的に実現可能な展望であることを示唆している。
倫理的、臨床的、およびシステム的な影響
有効性と安全性以外にも、社会的な問いが存在する。複雑で高価になる可能性のあるナノ医薬品の費用は誰が負担するのか。公平なアクセスをどのように確保するのか。外部から操作されるデバイスが意図しない損傷を引き起こした場合、どのような責任の枠組みが適用されるのか。科学的に厳格で社会的に責任ある形で治験や展開を形作るためには、技術者、臨床医、規制当局、および倫理学者の間での早期の対話が必要となるだろう。
結論:明日の治療法ではないが、信頼に足るツールキット
細胞毒性ペプチドを隠すpH活性化DNAオリガミから、トロンビンを露出させるナノデバイス、肺転移に薬剤を届けるバイオハイブリッド・スイマーまで、最近発表された一連の論文やプレスリリースは、一つの収束する傾向を示している。エンジニアと生物学者は、生体組織内で感知、局在化、活動が可能な、プログラム可能で注入可能な構築物を組み立てつつある。これらの能力は、真の技術的進歩を象徴している。同時に、マウスから医薬品への道は長く、それぞれの設計には独自の技術的および規制的な難題が伴う。今後数年間は、まず最も安全でシンプルな設計の慎重で段階的な臨床試験が行われ、その一方で、より野心的で多機能なナノロボットが前臨床研究室で成熟し続けることが期待される。
Sources
- Nature Nanotechnology (paper on pH‑activated DNA nanostructures)
- Karolinska Institutet (press release and research materials)
- Nature Biotechnology (DNA nanorobot delivering thrombin)
- Science Advances / University of California San Diego (microrobots for metastatic lung tumours)
- Advanced Science / University of Illinois Urbana‑Champaign (DNA origami imaging and targeting for pancreatic cancer)
Comments
No comments yet. Be the first!