やかんの音に応える子供:見出しを塗り替えたささやかな瞬間
彼女は台所のシンクから母親に応えた。それは臨床的な金字塔というよりも、親が大切に取っておくような、ありふれた日常の一コマだった。たった1度の手術から4か月後、その7歳の少女は家庭内での会話についていくことができ、やかんの音も聞こえるようになった。この光景はプレスリリースや見出しで繰り返し引用され、「難聴の回復」という言葉を後押しした。1回の注入で、科学者が10人の患者の聴力を回復させたのである。これは治験で報告された内容を正確に描写したものであるが、同時に、この単純なストーリーだけでは不十分な点も出てくる。
「難聴の回復」:科学者による修復 ―― 見出しを飾る数字
この治験には1歳から24歳までの10人の参加者が登録された。この集団全体で、患者が感知できる平均音圧レベルは、6か月以内に約106デシベルから52デシベルへと低下した。これは、極度の難聴から、多くの人にとって日常会話が可能な範囲へと変化したことを意味する。改善はしばしば迅速で、複数の患者がわずか1か月後には機能を示し始め、最年少の子供たち(特に5歳から8歳)で最も大きな効果が見られた。ある7歳の子供は機能的な聴力をほぼ完全に取り戻し、電話で話したり家族と日常会話を交わしたりできるようになった。
これらの数字は、なぜメディアが「難聴の回復」という言葉を掲げ、なぜ親や臨床医が熱狂しているのかを説明している。同時に、そこには明らかな統計上の注意点も含まれている。10人という数は依然として小規模なサンプルである。この研究はランダム化比較対照のない単群試験であり、これまでの追跡調査は年単位ではなく月単位に留まっている。この結果は、この特定の変異に対する生物学的な妥当性を強力に証明するものではあるが、まだ万能な治療法ではない。
「難聴の回復」:科学者による修復 ―― OTOFに限定されるという重要性
治療を受けた患者はすべて、同じ分子診断を共有していた。それは、内有毛細胞から聴神経への音情報のシナプス伝達に不可欠なタンパク質であるオトフェリンをコードする遺伝子、OTOFにおける両アレル性機能喪失変異である。これらの有毛細胞に正常なOTOFのコピーを届けることで、その伝達が回復し、報告されたような測定可能な改善がもたらされた。
手術の瞬間と論文で報告された生物学的知見
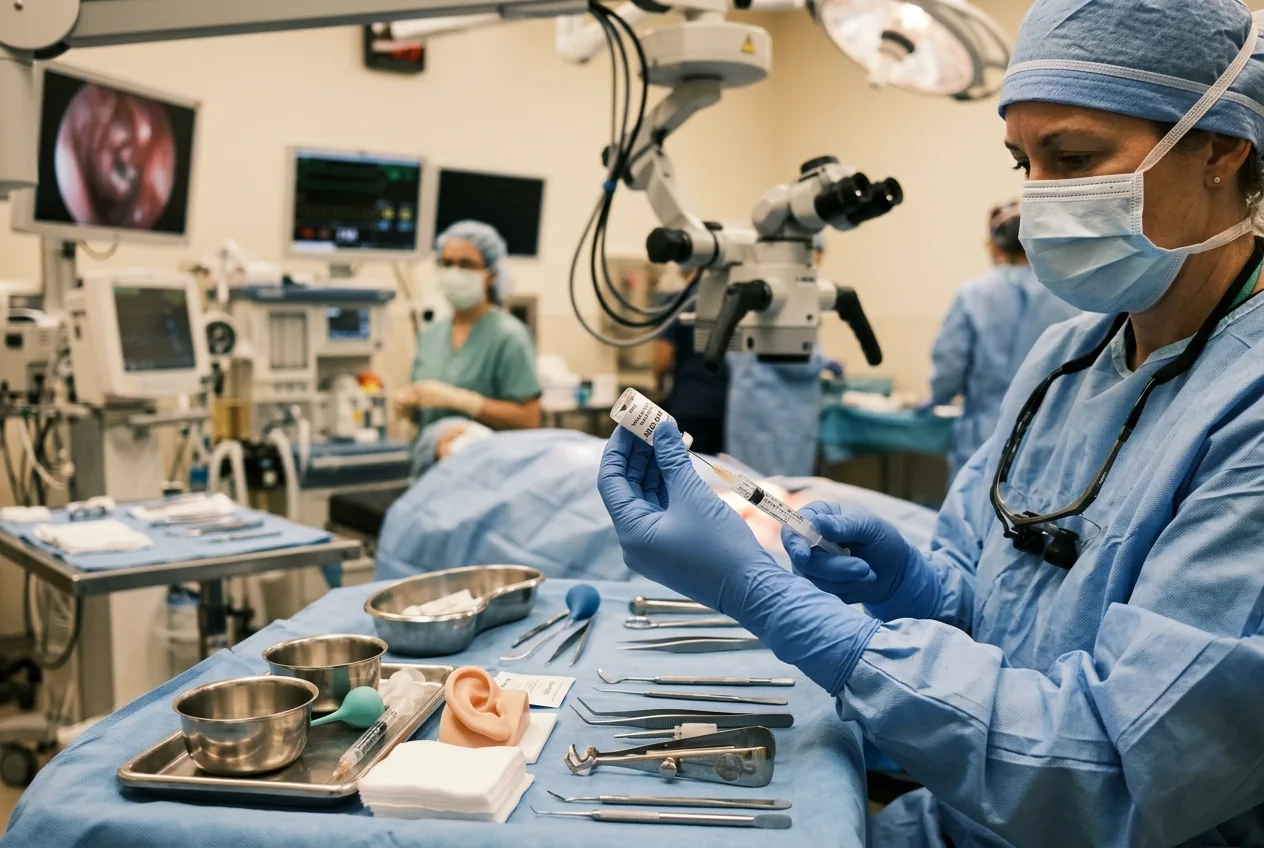
この治験の手順は外科的かつ局所的なもので、臨床医は機能的なOTOF配列を搭載したAAVベースのベクターを、正円窓膜を通して蝸牛(かぎゅう)内に注入した。内耳は閉鎖された繊細な空間であり、手術には耳科手術の技術と画像診断が必要となる。治験チームの報告によると、介入は概ね良好に許容された。臨床検査における最も一般的な変化は一時的な好中球数の減少であり、決定的な点として、6か月から12か月の追跡期間中に重篤な有害事象は報告されなかった。
その安全性プロファイルは今後も注視していく必要がある。アデノ随伴ウイルス(AAV)ベクターは、比較的安全であるため遺伝子治療で広く使用されているが、蝸牛の容量の小ささと、治療対象となる細胞が中枢神経系に近いことから、投与量、免疫反応、長期的な発現について特有の疑問が生じる。この治験も論文も、その効果が数年、数十年にわたってどの程度持続するのか、反復投与が必要になるのか、あるいは両耳投与が片耳投与と比較してどのようなパフォーマンスを示すのかについては、まだ答えることができない。
商業的関係、対立、そして一般的な難聴治療への競争
対立関係以外にも、より構造的な緊張が存在する。遺伝性難聴の各形態には、新しいベクター、新しい製造法、オーダーメイドの手術プロトコル、そして新たな安全性データといった、それぞれに合わせた個別の治療法が必要となる。このような特注の性質があるからこそ、University of SheffieldのRinri Therapeuticsを含む多くのグループが、より広範な感音難聴を対象とした、幹細胞由来の聴神経前駆細胞を開発するという異なるアプローチを追求している。細胞治療はより幅広い適用性を約束するが、それ特有の規制、製造、供給におけるハードルを伴う。経済状況は厳しい。個別化された遺伝子治療薬や複雑な細胞製剤は、開発とスケールアップに多大な費用がかかる。誰が費用を負担するのか、そして規制当局がいかに迅速に新しいアプローチを受け入れるのか、という問いは未解決のままである。
この治療法は今すぐ利用できるのか ―― そして本当のリスクとは?
端的な答えは「ノー」だ。日常的な臨床使用はまだできない。Nature Medicine誌の治験は、初期の臨床段階にある。製品は依然として実験段階にあり、より広範な承認への道には、持続的な有益性、多様な集団における許容可能な安全性、再現性のある製造、そしてコストとアクセスに関する明確さを示す大規模な多施設共同試験が必要となる。見出しを目にする家族にとって、これは受け入れがたいメッセージかもしれない。科学は本物であり、これらの患者に対して治療は効果を発揮したが、一般の人々が利用できるようになるには、さらなる治験と規制当局による審査が必要なのである。
リスクに関しては、公表された追跡調査では最初の1年間に重篤な副作用は見られなかったが、臨床医や規制当局は、遅発性の免疫影響、オフターゲット発現、そして遺伝的修復後の長期的な蝸牛生物学における未知の要素を監視することになる。また、蝸牛にアプローチするという実務上の外科的リスクや、高齢で治療を受けた患者は、長期間の神経剥奪(刺激の欠如)のために子供よりも得られる効果が少ない可能性もある。
何百万人もの聴力回復に向けた長い道のりにおける今回の位置づけ
今回の治験は転換点である。遺伝子治療がヒトの蝸牛内に安全に届けられ、特定の遺伝的サブグループに対して迅速かつ意味のある改善をもたらすことができると証明した。これは稀有で重要なことだ。しかし、医学の歴史は、一般化が困難であると判明した初期の奇跡で溢れている。次のステップは、製造のスケールアップ、ランダム化試験の実施、複数の国や地域での規制当局の承認取得、そして新しいクラスの治療法を提供し監視するための外科・聴覚システムの構築といった、実務的で高額な費用の掛かる、息の長い作業になるだろう。
一方で、RinriのRincell-1ニューロン置換プログラムのような補完的な道は、加齢や騒音被害による感音難聴という、より大きな市場を目指している。これらの技術が成功すれば、より多くの人々に届く可能性があるが、独自の実証実験や供給上のハードルに直面することになる。差し当たっての教訓は、この分野が現在、特定の単一遺伝子性難聴を対象とした標的遺伝子修正と、後天性または複雑な形態を対象とした広範な再生アプローチという、正当な二極化を遂げているということだ。
台所のやかんは、今でもその意義を測る良い指標である。治験の参加家族にとって、1度の手術は数か月のうちに人生を変えるような変化をもたらした。世界の他の人々にとって、「難聴の回復:科学者による修復」という見出しは、完結した物語ではなく、進行中の約束である。今求められている入念な作業は、持続性、規模、公平性、そして独立した再現性に関するものであり、非常に実際的な問いは、規制当局や医療システムが、このエレガントで遺伝子特異的な成功を、それを必要とする人々への公平で永続的なアクセスへと変えられるかどうかなのである。
Sources
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (press materials and institutional research communications)
- Zhongda Hospital, Southeast University (clinical collaborators)
- Rinri Therapeutics / University of Sheffield (Rincell‑1 and regenerative cell therapy programme)
- Otovia Therapeutics (developer and funder involved in the trial)
Comments
No comments yet. Be the first!