Araştırmacılar belirli işitme kayıpları için şaşırtıcı bir moleküler kurtarma yolu buldu
Bu yıl önde gelen bir klinik dergide yayımlanan makalede, University of Chicago liderliğindeki uluslararası bir ekip, konjenital sensörinöral işitme kaybının genetik bir nedenini belirledi ve daha da önemlisi, laboratuvar modellerinde bu hasarı geri döndürmenin yollarını gösterdi. Bu durumun sorumlusunun CPD geninin daha önce yeterince önemsenmeyen bir rolü olduğu saptandı; test edilen tedavi yöntemleri ise L-arginin takviyelerini ve en çok erektil disfonksiyon tedavisiyle tanınan ilaçların etken maddesi olan sildenafili içeriyor.
Ekibin keşfettikleri
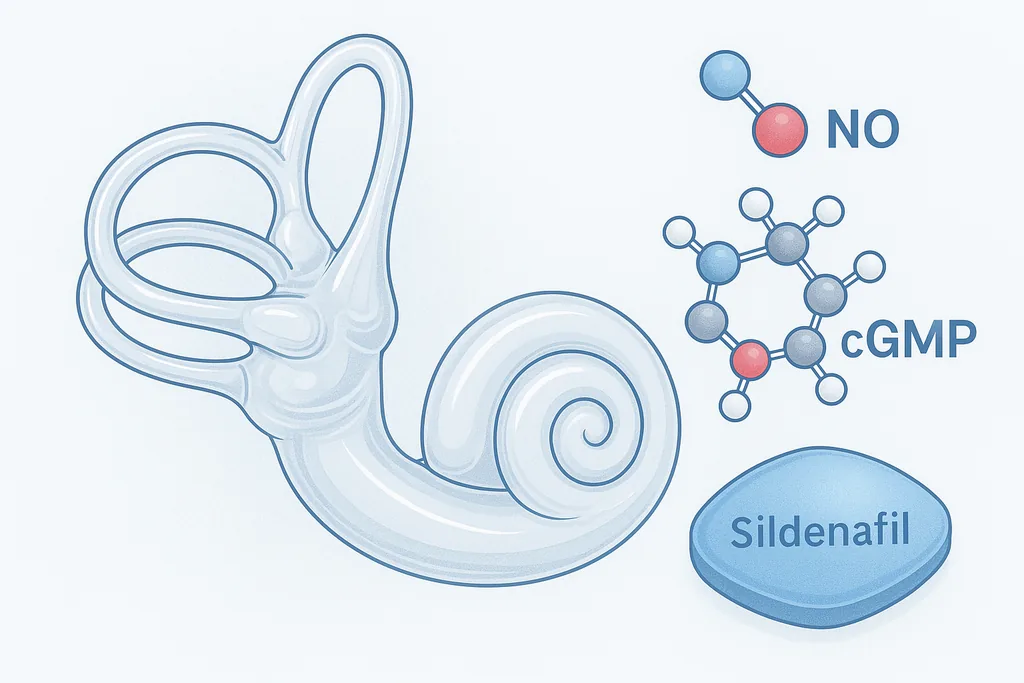
Hücresel düzeyde, CPD aktivitesinin, nitrik oksit (NO) üretmek için gereken amino asit substratı olan argininin korunması için önemli olduğu ortaya çıktı. İç kulağın hassas duyusal tüy hücrelerinde CPD kaybı, arginin mevcudiyetini ve akış aşağı NO sinyallemesini azaltıyor. Bu eksiklik hücresel stresi artırıyor ve birçok sensörinöral işitme kaybı formunun temelinde yatan geri dönüşü olmayan hasar olan tüy hücresi ölümüyle sonuçlanan yolakları tetikliyor.
Sildenafil biyolojiye nasıl dahil oluyor?
Nitrik oksit, diğer etkilerinin yanı sıra siklik GMP (cGMP) üretimini uyaran bir sinyal molekülü olarak görev yapar. Fosfodiesterazlar (PDE'ler) olarak bilinen enzimler cGMP'yi parçalar; sildenafil bu enzimlerden birini (PDE5) inhibe ederek cGMP sinyallemesini etkili bir şekilde artırır. Çalışmada ekip, cGMP'yi artırmanın CPD eksikliğinin neden olduğu azalmış NO üretimini telafi edebileceğini varsaydı.
Hasta kaynaklı kültürlenmiş hücrelerde, organotipik fare koklear preparatlarında ve CPD kaybına sahip meyve sineği modellerinde, arginin takviyesi yapmak veya sildenafil ile cGMP yolağını farmakolojik olarak güçlendirmek, hücre hayatta kalmasını iyileştirdi ve işitme fonksiyonunu kısmen geri kazandırdı. Sineklerde, işitme ve denge ile ilgili davranışsal ölçümler düzeldi. Koklear kültürlerde ve hücre sistemlerinde, arginin veya sildenafil uygulandığında oksidatif ve endoplazmik retikulum stresi belirteçleri azaldı.
Bu neden dikkate değer?
- Tanımlanmış bir moleküler mekanizma: Çalışma, tek bir biyokimyasal yolağı — arginin → nitrik oksit → cGMP — tüy hücresi sağlığına bağlayarak müdahale için net bir hedef sunuyor.
- Genetik bir sağırlık formu için terapötik potansiyel: Hiçbir ilaç tedavisinin hasarı geri döndüremediği çoğu sensörinöral işitme kaybının aksine, bu form modellerde biyokimyasal kurtarmaya uygun görünüyor.
- Bilinen bir ilacın yeniden amaçlandırılması: Sildenafil halihazırda diğer kullanımlar için FDA onaylı olduğundan, laboratuvardan klinik testlere giden yol, tamamen yeni bir bileşiğe göre daha hızlı olabilir — ancak bu hız, aşağıda açıklanan çekinceleri de beraberinde getiriyor.
Önemli çekinceler ve yanıtlanmamış sorular
Vaat ettiklerine rağmen, sildenafilin bir işitme tedavisi olarak görülmesinden önce birkaç neden dikkatli olunmasını gerektiriyor.
- Nadir, spesifik mutasyonlar: Deneyler CPD işlev kaybı varyantlarını hedefliyor. Popülasyondaki işitme kayıplarının çoğu yaşa bağlı veya gürültü kaynaklıdır ve karmaşık nedenlere sahiptir; CPD varyantlarının tarif edilen ailelerin ötesinde insan sağırlığına ne kadar yaygın katkıda bulunduğu henüz bilinmiyor.
- Model sistemler insan değildir: Ekip fareleri, kültürlenmiş insan hücrelerini ve meyve sineklerini kullandı. Bunlar mekanizma kurmak ve kavram kanıtlama için güçlü araçlardır, ancak güvenliği, dozajı, insan iç kulağına dağılımı veya uzun vadeli etkileri tam olarak öngöremezler.
- Sistemik vs yerel dozaj: Sildenafil vücut genelinde dolaşır. İç kulak için etkili dozların sistemik olarak güvenli olup olmayacağı veya kokleaya yerel uygulama gerekip gerekmeyeceği belirsizliğini koruyor. İç kulak, ilaç erişiminin ve konsantrasyonunun diğer dokulardan büyük ölçüde farklılık gösterdiği küçük, sıkıca mühürlenmiş bir organdır.
- Karmaşık önceki kanıtlar: Son on yıldaki hayvan araştırmaları, PDE5 inhibitörlerinin farklı koşullar altında işitmeyi koruyup korumadığı veya zarar verip vermediği konusunda karışık sinyaller verdi. Bazı çalışmalar gürültü veya patlama modellerinde koruyucu etkiler rapor ederken; diğerleri hiçbir değişiklik göstermiyor. İnsanlarda, PDE5 inhibitörleri ile ani işitme değişiklikleri bildiren nadir vaka raporları vardır, ancak popülasyon düzeyindeki kanıtlar tutarsızdır. Kapsamlı klinik değerlendirme gerekli olacaktır.
Sırada ne var?
Böyle bir çalışmadan klinik kullanıma giden tipik yol birkaç adım içerir. Araştırmacılar önce daha geniş işitme kaybı kohortlarında CPD varyantlarının ne kadar yaygın olduğunu doğrulamalı ve kısmi CPD fonksiyonunun veya tek kopya varyantların ilerleyen yaşlardaki işitme kaybına yatkınlığı artırıp artırmadığını belirlemelidir. Sırada dozajı, uygulama yöntemini ve zamanlamayı optimize etmek için preklinik çalışmalar, ardından hemen işitme restorasyonundan ziyade kulaktaki güvenlik ve biyolojik aktiviteye odaklanan dikkatle tasarlanmış erken insan deneyleri yer alıyor.
Eğer erken insan çalışmaları güvenli bir dozaj aralığı ve ilacın koklear hedeflere ulaştığına dair kanıt bulursa, o zaman küçük etkililik denemeleri; arginin takviyesinin, sistemik sildenafilin veya hedeflenmiş koklear uygulamanın, doğrulanmış CPD kaynaklı eksiklikleri olan kişilerde işitmeyi iyileştirip iyileştirmediğini veya ilerlemeyi yavaşlatıp yavaşlatmadığını test edebilir. Sildenafil zaten diğer endikasyonlar için onaylanmış olsa da, düzenleyici kurumlar herhangi bir yeni kullanım için yine de spesifik güvenlik ve etkililik verileri talep edecektir.
Genel sonuçlar ve çıkarımlar
Spesifik CPD hikayesinin ötesinde, bu çalışma modern biyomedikal araştırmalardaki iki geniş eğilimi örneklemektedir. Birincisi, genetik dedektiflik — nadir ailesel vakaları moleküler yolaklara bağlamak — popülasyon düzeyindeki çalışmalarda gözden kaçan ilaçla hedeflenebilir hassasiyetleri ortaya çıkarabilir. İkincisi, moleküler anlayışa dayalı olarak mevcut ilaçları yeniden amaçlandırmak, biyoloji net olduğunda ve ilacın güvenlik profili iyi karakterize edildiğinde verimli bir translasyonel stratejidir.
Ben James Lawson, Dark Matter için bildiriyorum. Bu araştırma, modern genetik ve moleküler sinirbilim merceğinden incelendiğinde, yerleşik ilaçların bazen şaşırtıcı yeni kullanım alanları bulabileceğini hatırlatıyor.
Comments
No comments yet. Be the first!