Ребенок, откликнувшийся на свист чайника: мгновение, изменившее смысл заголовка
Она ответила матери, стоя у кухонной раковины: это не клиническая веха, а обычная бытовая сцена, которую родители бережно хранят в памяти. Спустя четыре месяца после единственной операции семилетняя девочка смогла поддерживать разговор дома — она услышала чайник. Этот образ неоднократно тиражировался в пресс-релизах и заголовках, подпитывая фразу «глухота побеждена»: ученые восстановили слух у 10 пациентов после одной инъекции. Это точное описание результатов испытания, но именно здесь простая история перестает быть исчерпывающей.
«Глухота побеждена»: ученые восстанавливают слух — цифры, создающие заголовки
В испытании приняли участие десять человек в возрасте от 1 до 24 лет. В рамках когорты средний уровень звука, который могли воспринимать пациенты, снизился со 106 децибел до 52 децибел в течение шести месяцев — сдвиг, переводящий экстремальную потерю слуха в диапазон, где для многих возможна разговорная речь. Улучшения часто наступали быстро: у нескольких пациентов функция начала проявляться уже через месяц, а наибольший прогресс наблюдался у самых маленьких детей — особенно в возрасте от пяти до восьми лет. Один семилетний ребенок восстановил практически полный функциональный слух и смог разговаривать по телефону и вести повседневные беседы с семьей.
Эти цифры объясняют, почему пресса использовала слова «глухота побеждена» и почему родители и клиницисты воодушевлены. Они также содержат очевидную статистическую оговорку: десять человек — это все еще небольшая выборка. Исследование является одногрупповым испытанием без рандомизированного контроля, а последующее наблюдение пока ограничено месяцами, а не годами. Результат является мощной демонстрацией биологической обоснованности метода для этой конкретной мутации, но пока не универсальным лекарством.
«Глухота побеждена»: ученые восстанавливают слух — ограничение геном OTOF, и это важно
Все пролеченные пациенты имели одинаковый молекулярный диагноз: биаллельные мутации с потерей функции в OTOF — гене, кодирующем отоферлин, белок, критически важный для синаптической передачи звуковой информации от внутренних волосковых клеток к слуховому нерву. Доставка исправной копии OTOF в эти волосковые клетки восстановила эту связь и привела к зафиксированным в отчете улучшениям.
Операционный момент и биологические данные, описанные в статье
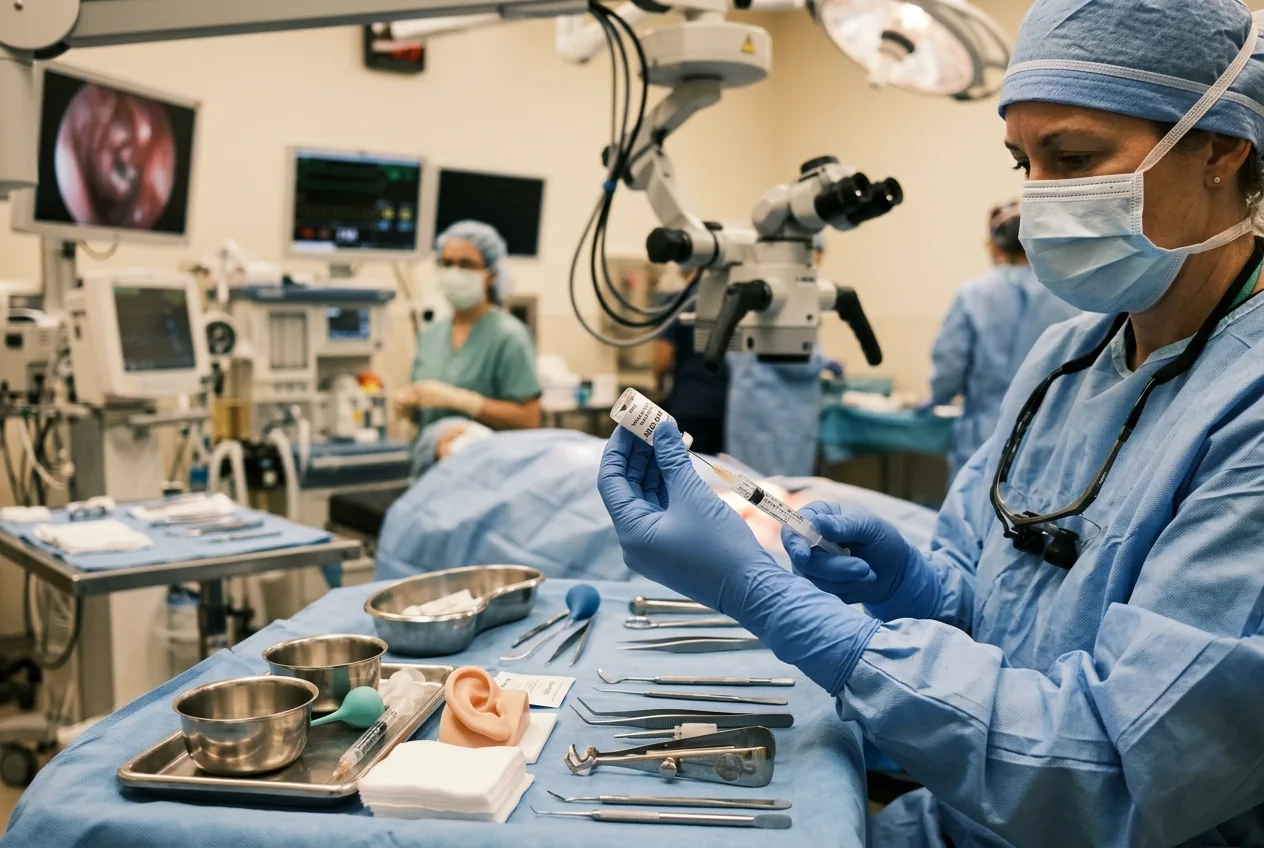
Процедура в ходе испытания была хирургической и локальной: клиницисты вводили вектор на основе AAV, несущий функциональную последовательность OTOF, через мембрану круглого окна в улитку. Внутреннее ухо — это замкнутое, деликатное пространство; операция требует навыков отохирургии и визуализации. Команды испытателей сообщают, что вмешательство в целом переносилось хорошо. Самым частым лабораторным изменением стало временное снижение количества нейтрофилов, и, что крайне важно, за период наблюдения от 6 до 12 месяцев не было зарегистрировано никаких серьезных нежелательных явлений.
За этим профилем безопасности нужно будет внимательно следить. Аденоассоциированные вирусные векторы широко используются в генной терапии, так как они сравнительно безвредны, но малый объем улитки и близость обрабатываемых клеток к центральной нервной системе ставят специфические вопросы о дозе, иммунном ответе и долгосрочной экспрессии. Ни испытание, ни статья пока не могут дать ответ на вопрос о том, насколько стойким будет эффект на протяжении десятилетий, потребуется ли повторное введение доз и как двустороннее (в оба уха) лечение соотносится с односторонним.
Коммерческие связи, конфликты и гонка за лечением распространенных форм глухоты
Помимо конфликтов интересов, существует и более системное напряжение. Каждая генетическая форма глухоты потребует своего индивидуального лечения: новых векторов, нового производства, специальных хирургических протоколов и новых досье безопасности. Именно эта специфика заставляет многие группы — включая Rinri Therapeutics при University of Sheffield — пробовать другой путь, разрабатывая полученные из стволовых клеток предшественники слухового нерва, нацеленные на более широкий класс сенсоневральных потерь слуха. Клеточная терапия обещает более широкую применимость, но несет в себе собственные нормативные, производственные и логистические трудности. Экономика сурова: разработка и масштабирование персонализированных генных препаратов и сложных клеточных продуктов обходятся дорого. Кто будет платить и как быстро регуляторы примут новые подходы, остается открытым вопросом.
Доступно ли лечение сейчас — и каковы реальные риски?
Краткий ответ: нет, не для рутинного клинического использования. Испытание, опубликованное в Nature Medicine, — это ранний клинический шаг. Продукт остается экспериментальным, а путь к широкому одобрению предполагает более крупные многоцентровые испытания, которые продемонстрируют стойкую пользу, приемлемую безопасность в различных популяциях, воспроизводимое производство и ясность в вопросах стоимости и доступа. Для семей, читающих заголовки, это может быть неприятным сообщением: наука реальна, и терапия сработала для этих пациентов, но доступность для широкой публики потребует дополнительных испытаний и регуляторного надзора.
Что касается рисков, то опубликованные данные наблюдения не выявили серьезных побочных реакций в первый год, но врачи и регуляторы будут следить за отложенными иммунными эффектами, внетаргетной экспрессией и неизвестными факторами долгосрочной биологии улитки после генетического восстановления. Существует также практический хирургический риск при доступе к улитке и вероятность того, что пациенты, получающие лечение в более старшем возрасте, получат меньше пользы, чем дети, из-за длительной нейронной депривации.
Место этого достижения в долгосрочном процессе восстановления слуха для миллионов людей
Данное испытание является переломным моментом: оно доказывает, что генная терапия может быть безопасно доставлена в человеческую улитку и давать быстрые, значимые результаты для генетической подгруппы. Это редкость и это важно. Но история медицины полна ранних «чудес», которые оказалось трудно масштабировать. Следующие шаги будут прагматичными, дорогими и медленными: масштабирование производства, проведение рандомизированных испытаний, получение разрешений регулирующих органов в различных юрисдикциях и создание хирургических и аудиологических систем для применения и мониторинга нового класса методов лечения.
Между тем, дополнительные направления, такие как программа замены нейронов Rincell-1 от компании Rinri, нацелены на более крупный рынок сенсоневральной тугоухости, вызванной старением и воздействием шума. Эти технологии, в случае успеха, смогут охватить больше людей, но столкнутся с собственными препятствиями на этапе доказательства концепции и доставки. Ближайший урок заключается в том, что область теперь законно разделилась на два направления: точечные генетические исправления для конкретной моногенной глухоты и более широкие регенеративные подходы для приобретенных или сложных форм.
Кипящий чайник на кухне — по-прежнему хороший способ измерить значимость достигнутого. Для семей участников испытания одна операция привела к изменениям, меняющим жизнь, всего за несколько месяцев. Для остального мира заголовок «Глухота побеждена»: ученые восстанавливают слух — это скорее обещание в процессе реализации, чем законченная история. Сейчас предстоит тщательная работа над долговечностью эффекта, масштабируемостью, справедливостью доступа и независимым воспроизведением результатов; практический вопрос заключается в том, смогут ли регуляторы и системы здравоохранения превратить элегантный, генно-специфичный успех в честный и постоянный доступ для тех, кто в нем нуждается.
Источники
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (пресс-материалы и сообщения о ведомственных исследованиях)
- Zhongda Hospital, Southeast University (клинические партнеры)
- Rinri Therapeutics / University of Sheffield (программа Rincell-1 и регенеративная клеточная терапия)
- Otovia Therapeutics (разработчик и спонсор, участвовавший в испытании)
Comments
No comments yet. Be the first!