Uma criança respondendo à chaleira: o pequeno momento que reformulou uma manchete
Ela respondeu à mãe da pia da cozinha: não um marco clínico, mas o tipo de cena comum que os pais guardam consigo. Quatro meses após uma única operação, a criança de sete anos conseguia acompanhar uma conversa em casa — ela conseguia ouvir a chaleira. Essa imagem foi repetidamente reciclada por materiais de imprensa e manchetes, e ajudou a impulsionar a frase "surdez revertida": cientistas restauram a audição em 10 pacientes após uma única injeção. É uma descrição precisa do que o ensaio relatou, e é também onde a história simples deixa de ser suficiente.
"surdez revertida": cientistas restauram — os números que geram manchetes
O ensaio recrutou dez participantes com idades entre 1 e 24 anos. Em toda a coorte, o nível médio de som que os pacientes conseguiam perceber caiu de cerca de 106 decibéis para 52 decibéis em seis meses — uma mudança que converte a perda auditiva extrema em uma faixa onde a fala conversacional é possível para muitas pessoas. As melhorias foram frequentemente rápidas: vários pacientes começaram a mostrar funcionalidade após apenas um mês, e as crianças mais novas — particularmente aquelas entre cinco e oito anos — tiveram os maiores ganhos. Uma criança de sete anos recuperou quase totalmente a audição funcional e conseguiu falar ao telefone e manter conversas diárias com a família.
Esses números explicam por que a imprensa publicou as palavras "surdez revertida" e por que pais e clínicos estão entusiasmados. Eles também contêm uma ressalva estatística óbvia: dez pessoas ainda é uma amostra pequena. O estudo é um ensaio de braço único sem controle randomizado, e o acompanhamento até agora é limitado a meses em vez de anos. O resultado é uma demonstração poderosa da plausibilidade biológica para esta mutação específica, mas ainda não uma cura universal.
"surdez revertida": cientistas restauram — limitada ao OTOF, e isso importa
Os pacientes tratados compartilhavam o mesmo diagnóstico molecular: mutações bialélicas de perda de função no OTOF, o gene que codifica a otoferlina, uma proteína fundamental para a transferência sináptica de informações sonoras das células ciliadas internas para o nervo auditivo. A entrega de uma cópia correta do OTOF a essas células ciliadas restaurou essa comunicação e produziu as melhorias mensuráveis relatadas.
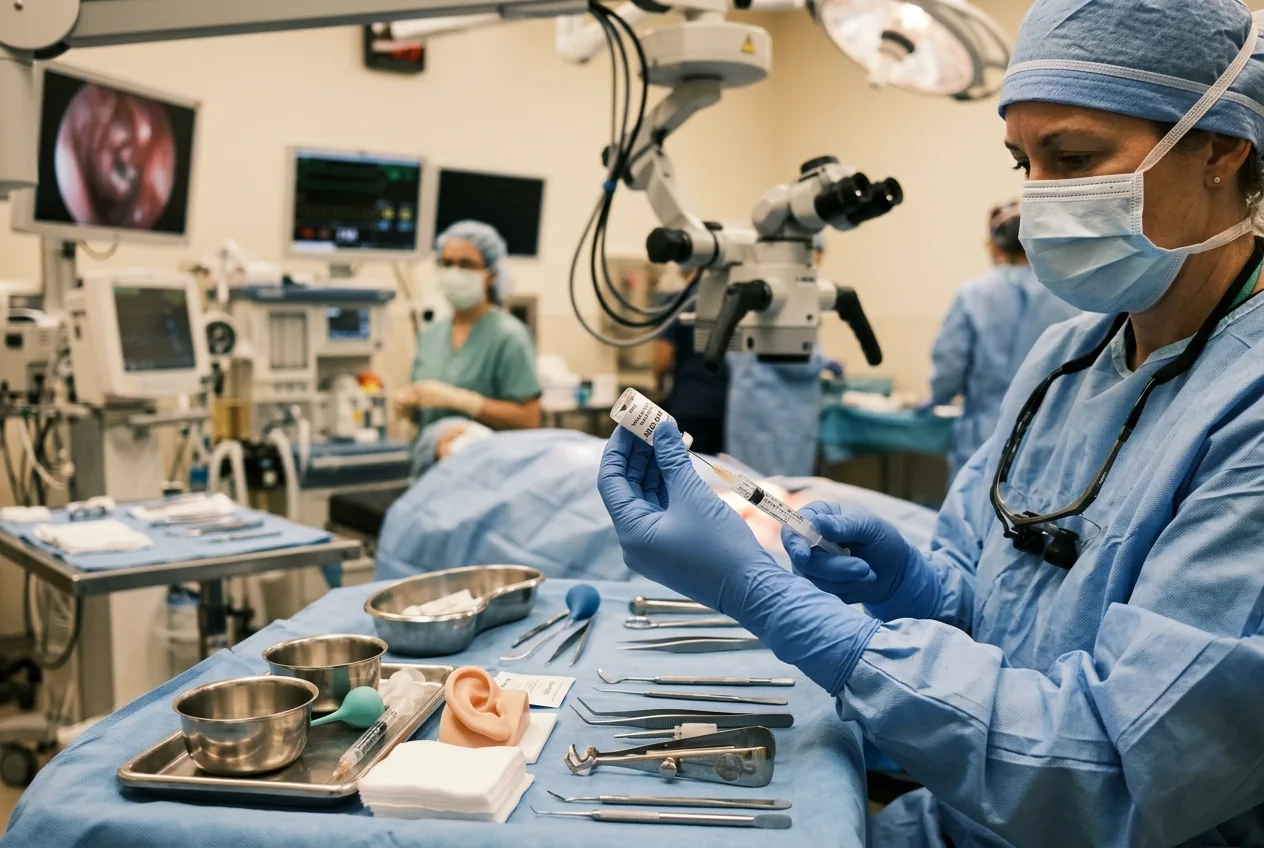
O momento operatório e a biologia relatada no artigo
O procedimento no ensaio foi cirúrgico e local: os clínicos injetaram um vetor baseado em AAV transportando uma sequência funcional de OTOF através da membrana da janela redonda para dentro da cóclea. O ouvido interno é um espaço confinado e delicado; a operação requer habilidade cirúrgica otológica e exames de imagem. As equipes do ensaio relatam que a intervenção foi, em geral, bem tolerada. A alteração laboratorial mais comum foi uma redução temporária na contagem de neutrófilos e, crucialmente, nenhum evento adverso grave foi relatado durante a janela de acompanhamento de seis a 12 meses.
Esse perfil de segurança precisará ser monitorado de perto. Vetores virais adeno-associados são amplamente utilizados em terapias gênicas por serem comparativamente benignos, mas o pequeno volume da cóclea e a proximidade das células tratadas com o sistema nervoso central levantam questões específicas sobre dose, resposta imune e expressão a longo prazo. Nem o ensaio nem o artigo podem responder ainda quão duradouro será o efeito ao longo de anos ou décadas, se doses repetidas serão necessárias ou como o tratamento bilateral (ambos os ouvidos) se comporta em comparação com a dosagem unilateral.
Laços comerciais, conflitos e a corrida para tratar a surdez comum
Além dos conflitos, há uma tensão mais sistêmica. Cada forma genética de surdez precisará de seu próprio tratamento personalizado: novos vetores, nova fabricação, protocolos cirúrgicos sob medida e novos dossiês de segurança. Essa natureza personalizada é o motivo pelo qual muitos grupos — incluindo a Rinri Therapeutics na University of Sheffield — estão seguindo um caminho diferente, desenvolvendo progenitores de nervo auditivo derivados de células-tronco visando uma classe mais ampla de perdas sensorineurais. As terapias celulares prometem uma aplicabilidade mais ampla, mas trazem seus próprios obstáculos regulatórios, de fabricação e de entrega. A economia é gritante: medicamentos gênicos personalizados e produtos celulares complexos são caros para desenvolver e escalar. Quem pagará e quão rápido os reguladores aceitarão as novas abordagens permanecem questões em aberto.
O tratamento está disponível agora — e quais são os riscos reais?
Resposta curta: não, não para uso clínico rotineiro. O ensaio da Nature Medicine é um passo clínico inicial. O produto continua sendo experimental, e o caminho para uma aprovação mais ampla envolve ensaios multicêntricos maiores que demonstrem benefício duradouro, segurança aceitável em diversas populações, fabricação reproduzível e clareza sobre custo e acesso. Para as famílias que ouvem as manchetes, essa pode ser uma mensagem desconfortável: a ciência é real e a terapia funcionou para esses pacientes, mas a disponibilidade ao público exigirá ensaios adicionais e revisão regulatória.
Quanto aos riscos, o acompanhamento publicado não mostrou reações adversas graves no primeiro ano, mas clínicos e reguladores estarão atentos a efeitos imunológicos tardios, expressão fora do alvo (off-target) e às incógnitas da biologia coclear a longo prazo após a restauração genética. Há também o risco cirúrgico prático de acessar a cóclea e a possibilidade de que pacientes que recebam o tratamento em idades mais avançadas ganhem menos do que as crianças devido à privação neural de longa data.
Onde isso se situa no arco mais longo em direção à restauração da audição para milhões
O ensaio é um ponto de inflexão: prova que uma terapia gênica pode ser entregue com segurança na cóclea humana e produzir ganhos rápidos e significativos para um subgrupo genético. Isso é raro e importante. Mas a história da medicina está repleta de milagres iniciais que se mostraram difíceis de generalizar. Os próximos passos serão pragmáticos, caros e lentos: escalar a fabricação, realizar ensaios randomizados, obter aprovação regulatória em múltiplas jurisdições e construir sistemas cirúrgicos e audiológicos para entregar e monitorar uma nova classe de tratamentos.
Enquanto isso, caminhos complementares, como o programa de substituição de neurônios Rincell-1 da Rinri, visam o mercado maior de perda sensorineural por envelhecimento e danos causados por ruído. Essas tecnologias, se tiverem sucesso, poderão atingir mais pessoas, mas enfrentarão seus próprios obstáculos de prova de conceito e entrega. A lição imediata é que a área está agora legitimamente bifurcada: correções gênicas direcionadas para surdez monogênica específica e abordagens regenerativas mais amplas para formas adquiridas ou complexas.
A chaleira em uma cozinha ainda é uma boa maneira de medir o significado. Para as famílias dos participantes do ensaio, uma única operação produziu mudanças que alteraram vidas em poucos meses. Para o resto do mundo, a manchete "surdez revertida": cientistas restauram é uma promessa em andamento, em vez de uma história finalizada. O trabalho cuidadoso agora é sobre durabilidade, escala, equidade e replicação independente; a questão muito prática é se os reguladores e sistemas de saúde podem converter um sucesso elegante e gene-específico em acesso justo e duradouro para aqueles que precisam.
Fontes
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (materiais de imprensa e comunicações de pesquisa institucional)
- Zhongda Hospital, Southeast University (colaboradores clínicos)
- Rinri Therapeutics / University of Sheffield (Rincell-1 e programa de terapia celular regenerativa)
- Otovia Therapeutics (desenvolvedora e financiadora envolvida no ensaio)
Comments
No comments yet. Be the first!