Una bambina che risponde al bollitore: il piccolo momento che ha ridefinito un titolo
Ha risposto a sua madre dal lavandino della cucina: non un traguardo clinico, ma il tipo di scena ordinaria che i genitori custodiscono gelosamente. Quattro mesi dopo un singolo intervento chirurgico, la bambina di sette anni era in grado di seguire una conversazione in casa — riusciva a sentire il bollitore. Quell'immagine è stata ripetutamente ripresa da comunicati stampa e testate, e ha contribuito ad alimentare l'espressione "sordità invertita": gli scienziati ripristinano l'udito in 10 pazienti dopo una singola iniezione. Si tratta di una descrizione accurata di quanto riportato dalla sperimentazione, ed è anche il punto in cui la narrazione semplice smette di essere sufficiente.
"sordità invertita": gli scienziati ripristinano l'udito — i numeri che fanno notizia
Lo studio ha arruolato dieci partecipanti di età compresa tra 1 e 24 anni. All'interno della coorte, il livello medio di suono percepibile dai pazienti è sceso da circa 106 decibel a 52 decibel nell'arco di sei mesi — un cambiamento che trasforma una perdita uditiva estrema in un range in cui il linguaggio parlato è possibile per molte persone. I miglioramenti sono stati spesso rapidi: diversi pazienti hanno iniziato a mostrare segni di funzionalità dopo appena un mese, e i bambini più piccoli — in particolare quelli tra i cinque e gli otto anni — hanno ottenuto i guadagni maggiori. Una bambina di sette anni ha recuperato un udito funzionale quasi completo ed è stata in grado di parlare al telefono e sostenere conversazioni quotidiane con la famiglia.
Questi dati spiegano perché la stampa abbia utilizzato l'espressione "sordità invertita" e perché genitori e medici siano entusiasti. Tuttavia, contengono anche un ovvio caveat statistico: dieci persone rappresentano ancora un campione ridotto. Lo studio è una sperimentazione a braccio singolo senza controllo randomizzato, e il follow-up finora è limitato a mesi piuttosto che ad anni. Il risultato è una potente dimostrazione della plausibilità biologica per questa specifica mutazione, ma non ancora una cura universale.
"sordità invertita": gli scienziati ripristinano l'udito — limitato all'OTOF, e questo è importante
I pazienti trattati condividevano tutti la stessa diagnosi molecolare: mutazioni bialleliche con perdita di funzione in OTOF, il gene che codifica l'otoferlina, una proteina fondamentale per il trasferimento sinaptico delle informazioni sonore dalle cellule ciliate interne al nervo uditivo. La somministrazione di una copia corretta di OTOF a quelle cellule ciliate ha ripristinato tale comunicazione, producendo i miglioramenti misurabili riportati.
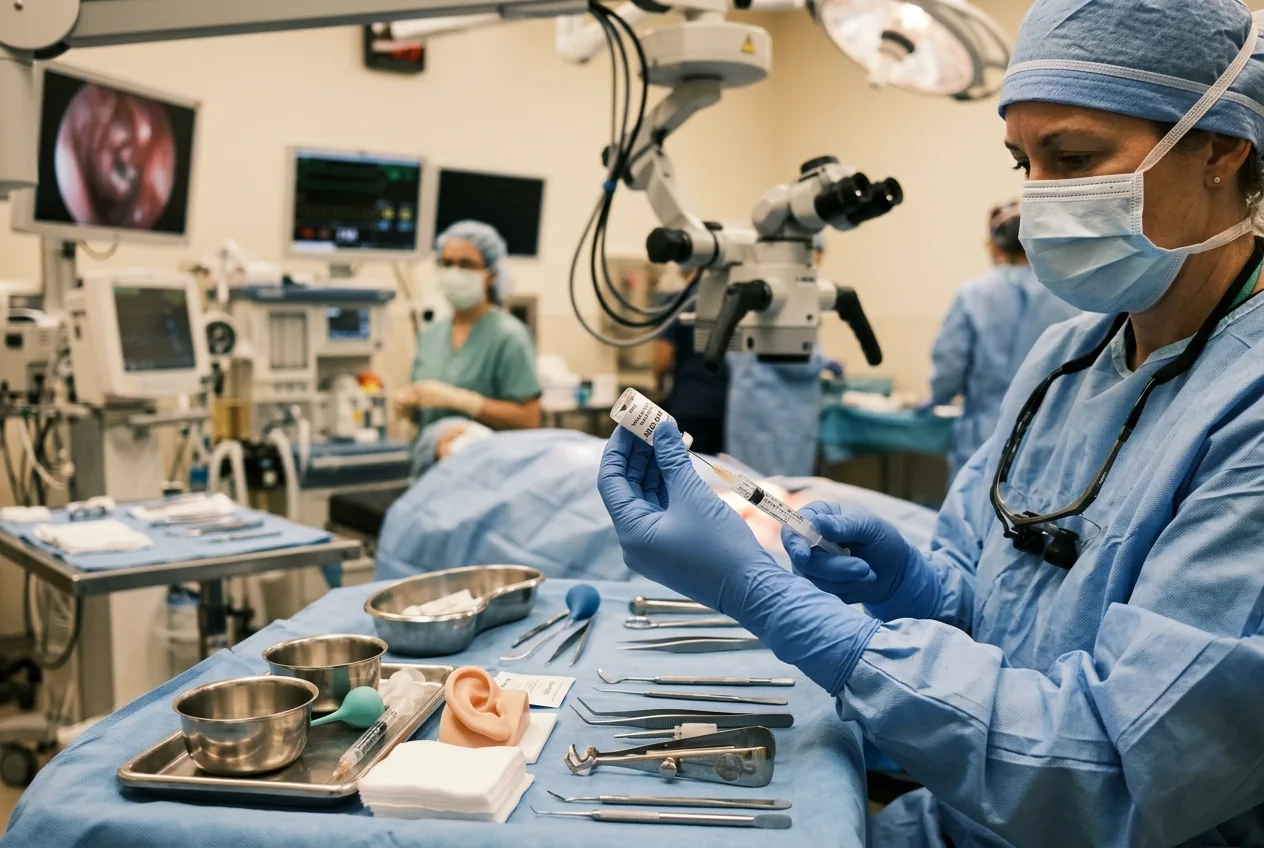
Il momento operatorio e la biologia riportata nello studio
La procedura della sperimentazione è stata chirurgica e locale: i medici hanno iniettato un vettore basato su AAV contenente una sequenza OTOF funzionale attraverso la membrana della finestra rotonda nella coclea. L'orecchio interno è uno spazio confinato e delicato; l'operazione richiede competenza chirurgica otologica e imaging. I team di ricerca riferiscono che l'intervento è stato generalmente ben tollerato. La variazione di laboratorio più comune è stata una riduzione temporanea della conta dei neutrofili e, cosa fondamentale, non sono stati segnalati eventi avversi gravi durante la finestra di follow-up da sei a 12 mesi.
Questo profilo di sicurezza dovrà essere monitorato attentamente. I vettori virali adeno-associati sono ampiamente utilizzati nelle terapie geniche perché relativamente benigni, ma il volume ridotto della coclea e la vicinanza delle cellule trattate al sistema nervoso centrale sollevano questioni specifiche su dosaggio, risposta immunitaria ed espressione a lungo termine. Né lo studio né l'articolo possono ancora rispondere a quanto l'effetto sarà duraturo nel corso di anni o decenni, se saranno necessari dosaggi ripetuti o come si comporti il trattamento bilaterale (entrambe le orecchie) rispetto a quello unilaterale.
Legami commerciali, conflitti e la corsa per trattare la sordità comune
Oltre ai conflitti, esiste una tensione più sistemica. Ogni forma genetica di sordità necessiterà di un proprio trattamento su misura: nuovi vettori, nuova produzione, protocolli chirurgici specifici e nuovi dossier di sicurezza. Questa natura personalizzata è il motivo per cui molti gruppi — tra cui Rinri Therapeutics presso l'University of Sheffield — stanno perseguendo una strada diversa, sviluppando progenitori del nervo uditivo derivati da cellule staminali mirati a una classe più ampia di perdite neurosensoriali. Le terapie cellulari promettono un'applicabilità più estesa, ma portano con sé ostacoli normativi, produttivi e di somministrazione. L'aspetto economico è netto: i farmaci genici personalizzati e i prodotti cellulari complessi sono costosi da sviluppare e scalare. Chi pagherà e quanto velocemente i regolatori accetteranno i nuovi approcci rimangono domande aperte.
Il trattamento è disponibile ora — e quali sono i rischi reali?
Risposta breve: no, non per l'uso clinico routinario. Lo studio di Nature Medicine è un primo passo clinico. Il prodotto rimane sperimentale e il percorso verso un'approvazione più ampia prevede studi multicentrici su vasta scala che dimostrino benefici duraturi, sicurezza accettabile in popolazioni diverse, produzione riproducibile e chiarezza su costi e accesso. Per le famiglie che leggono i titoli dei giornali, questo può essere un messaggio scomodo: la scienza è reale e la terapia ha funzionato per questi pazienti, ma la disponibilità per il pubblico richiederà ulteriori test e revisioni normative.
Per quanto riguarda i rischi, il follow-up pubblicato non ha mostrato reazioni avverse gravi nel primo anno, ma medici e autorità di regolamentazione monitoreranno eventuali effetti immunitari tardivi, espressione fuori bersaglio e le incognite della biologia cocleare a lungo termine dopo il ripristino genetico. Esiste anche il rischio chirurgico pratico legato all'accesso alla coclea e la possibilità che i pazienti trattati in età più avanzata ottengano meno benefici rispetto ai bambini a causa di una deprivazione neurale prolungata.
La collocazione di questo risultato nel lungo percorso verso il ripristino dell'udito per milioni di persone
La sperimentazione rappresenta un punto di svolta: prova che una terapia genica può essere somministrata in sicurezza nella coclea umana e produrre miglioramenti rapidi e significativi per un sottogruppo genetico. Questo è raro e importante. Ma la storia della medicina è costellata di miracoli precoci che si sono rivelati difficili da generalizzare. I prossimi passi saranno pragmatici, costosi e lenti: scalare la produzione, condurre studi randomizzati, ottenere l'approvazione normativa in più giurisdizioni e costruire sistemi chirurgici e audiologici per somministrare e monitorare una nuova classe di trattamenti.
Nel frattempo, percorsi complementari come il programma di sostituzione neuronale Rincell-1 di Rinri mirano al mercato più ampio della perdita neurosensoriale dovuta all'invecchiamento e ai danni da rumore. Tali tecnologie, se avranno successo, potrebbero raggiungere più persone, ma dovranno affrontare i propri ostacoli in termini di prova di concetto e somministrazione. La lezione immediata è che il campo è ora legittimamente biforcato: soluzioni geniche mirate per specifiche sordità monogeniche e approcci rigenerativi più ampi per forme acquisite o complesse.
Il bollitore in una cucina rimane un ottimo modo per misurare il significato dei risultati. Per le famiglie dei partecipanti alla sperimentazione, un singolo intervento ha prodotto cambiamenti che stravolgono la vita in pochi mesi. Per il resto del mondo, il titolo "sordità invertita": gli scienziati ripristinano l'udito è una promessa in divenire piuttosto che una storia conclusa. Il lavoro meticoloso ora riguarda la durata, la scala, l'equità e la replicazione indipendente; la questione pratica è se i regolatori e i sistemi sanitari riusciranno a convertire un elegante successo specifico per un gene in un accesso equo e duraturo per chi ne ha bisogno.
Fonti
- Nature Medicine (AAV gene therapy for autosomal recessive deafness 9: a single‑arm trial)
- Karolinska Institutet (materiali stampa e comunicazioni di ricerca istituzionali)
- Zhongda Hospital, Southeast University (collaboratori clinici)
- Rinri Therapeutics / University of Sheffield (Rincell‑1 e programma di terapia cellulare rigenerativa)
- Otovia Therapeutics (sviluppatore e finanziatore coinvolto nello studio)
Comments
No comments yet. Be the first!